Dolor inflamatorio vs a no inflamatorio
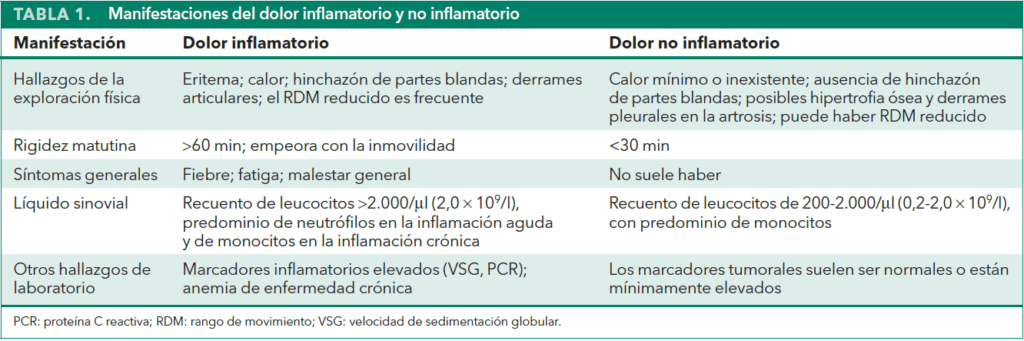
La diferenciación entre signos y síntomas inflamatorios y no inflamatorios es fundamental para la evaluación de los pacientes con dolor musculoesquelético. Los trastornos autoinmunes típicamente se presentan con inflamación, mientras que los trastornos mecánicos o degenerativos suelen ser no inflamatorios.
Los signos y síntomas básicos de inflamación son dolor, eritema, hinchazón y calor; con excepción del dolor, en general los trastornos no inflamatorios no cursan con estas manifestaciones. Cabe destacar que los pacientes pueden experimentar más de un tipo de dolor al mismo tiempo.
Exploración musculoesquelética
Una anamnesis precisa y una exploración física musculoesquelética exhaustiva son fundamentales para diagnosticar y diferenciar los síntomas inflamatorios y no inflamatorios y puede ayudar a evitar pruebas innecesarias.
El dolor musculoesquelético puede ser articular, periarticular o referido. El dolor con un rango de movimiento pasivo sugiere un trastorno no articular, mientras que el dolor con un rango de movimiento activo apunta a un trastorno periarticular.
Artritis
Monoartritis
La monoartritis afecta a una única articulación y se clasifica como aguda o crónica. La monoastritis agua puede ser no inflamatoria (traumatismo, hemartrosis o trastorno interno) o inflamatoria (inducida por cristales o infecciosa).
La evaluación para detectar artritis infecciosa debe basarse en la presentación clínica y la exploración, pero siempre con un grado alto de sospecha. Normalmente, la artrocentesis constituye el medio más eficaz para diagnosticar la causa subyacente.
La monoartritis inflamatoria crónica (>26 semanas) puede estar causada por una infección crónica (micobacteriana, fúngica o por Borrelia burgdoferi) o por una enfermedad reumática autoinmune.
El análisis del líquido sinovial confirmará la inflamación, pero puede ser insuficiente para el diagnóstico; es posible que haga falta una evaluación para buscar enfermedad sistémica (análisis serológicos y otras pruebas analíticas) y, en algunos casos, una biopsia sinovial.
Por lo general, la monoartrosis no inflamatoria crónica está causada por artrosis.
Oligoartrosis
La oligoartrosis afecta entre 2 o 4 articulaciones, normalmente en un patrón asimétrico. La oligoartrosis inflamatoria aguda puede estar causada por gonorrea o por fiebre reumática.
La oligoartrosis inflamatoria crónica puede deberse a trastornos autoinmunes como la espondiloartrosis.
Poliartrosis
La poliartrosis afecta a 5 o más articulaciones. En muchos casos, afecta a las articulaciones pequeñas de las manos y/o los pies. La poliartrosis aguda (<6 meses de evolución) puede estar causada por infecciones víricas (parvovirus B19, VIH, Virus de la Hepatitis B o rubéola) o representar una manifestación inicial de una poliartrosis inflamatoria crónica (>6 meses de evolución) como la artritis reumatoide (AR), el Lupus Eritematosos Sistémico (LES) o la artritis psoriásica.
Anomalías de partes blandas
Con frecuencia el origen de los síntomas musculoesqueléticos corresponden a las partes blandas (tendones, ligamentos y bolsas) situadas en torno a las articulaciones o lejos de estas.
Normalmente, la afectación de tendones y/o ligamentos aisladas es indicativa de trastornos no inflamatorios como lesión/irritación mecánica, sobrecarga o degeneración (trastorno del manguito de los rotadores o el codo del tenista). Los trastornos que comportan dolor musculoesquelético generalizado (como la fibromialgia) también cursan con síntomas localizados en estas estructuras.
La entesis es una estructura compleja situada en el lugar donde un tendón o ligamento se insertan en el hueso. La inflamación de la entesis (entesitis) es altamente indicativa de espondiloartrosis.
Cuando la entesis es especialmente grave, la inflamación puede extenderse a lo largo del tendón asociado y los ligamentos locales y dar lugar a dactilitis (dedos en salchicha).
Manifestaciones extraarticulares de enfermedad reumática
Síntomas generales
La fiebre, la rigidez matutina y la fatiga se dan en numerosos trastornos reumáticos. Por la común la fiebre es baja, aunque puede ser alta y con picos en algunos trastornos (enfermedad de Still del adulto y enfermedades autoinflamatorias).
La rigidez matutina de mas de 60 minutos de duración se observa sobre todo en la AR, pero también se presenta en otras formas de artritis inflamatoria. la fatiga significativa e incluso incapacitante es una manifestación prominente de la fibromialgia y el síndrome de fatiga crónica.
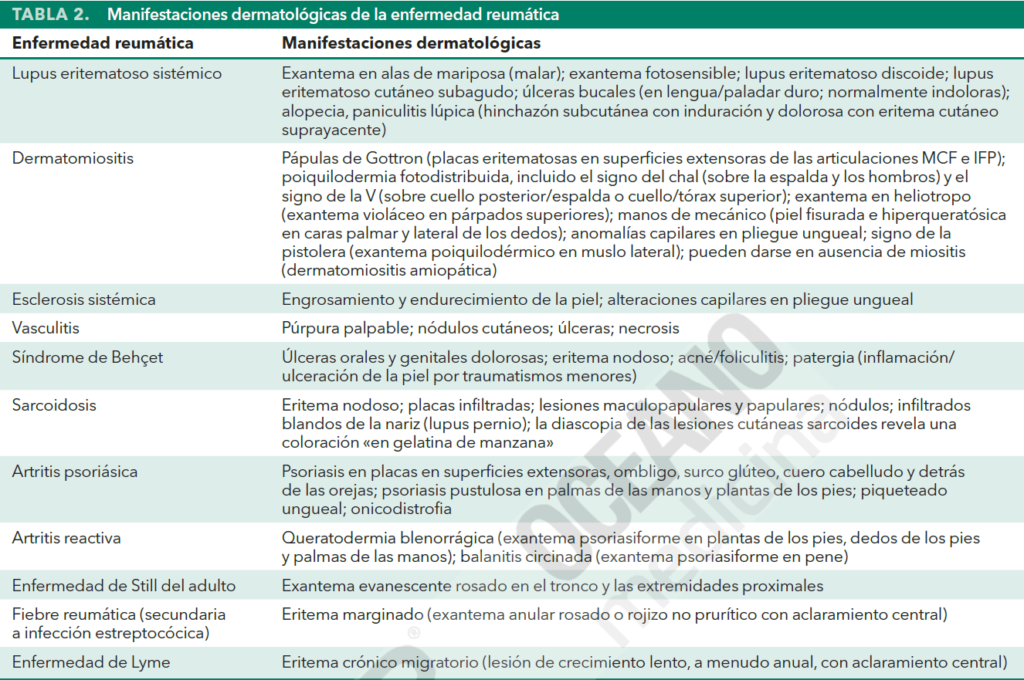
Afectación cutánea
Es frecuente en los trastornos reumáticos y puede pasar inadvertida por el paciente. Puede darse también como efecto adverso de los medicamentos empleados para tratar las enfermedades reumáticas, como pueden ser infecciones cutáneas secundarias a un tratamiento inmunosupresor.
Afectación ocular
Suele seguir patrones bastante definidos en diferentes enfermedades reumáticas, y la localización y el tipo de afectación puede ayudar a estrechar el diagnóstico diferencial. Si no se reconocen y trata con rapidez, algunas formas de afectación ocular pueden tener consecuencias devastadoras, entre ellas la ceguera permanente.
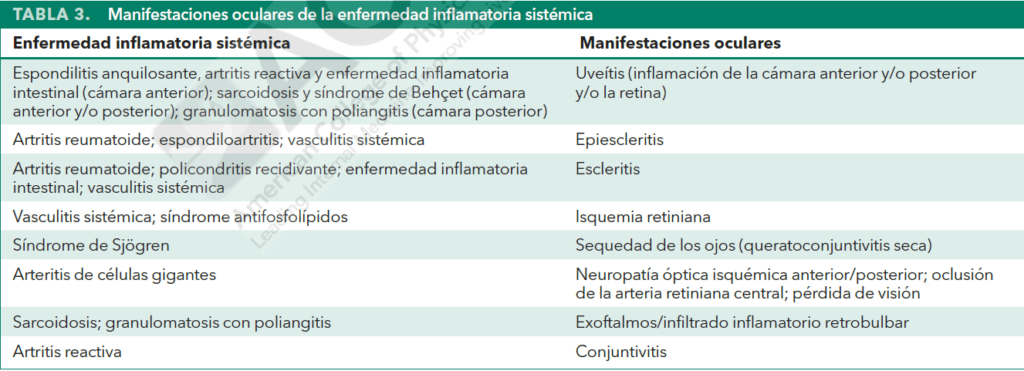
Afectación de órganos internos
Las enfermedades reumáticas afectan a menudo a órganos internos; las diferentes enfermedades tienden a seguir patrones característicos.
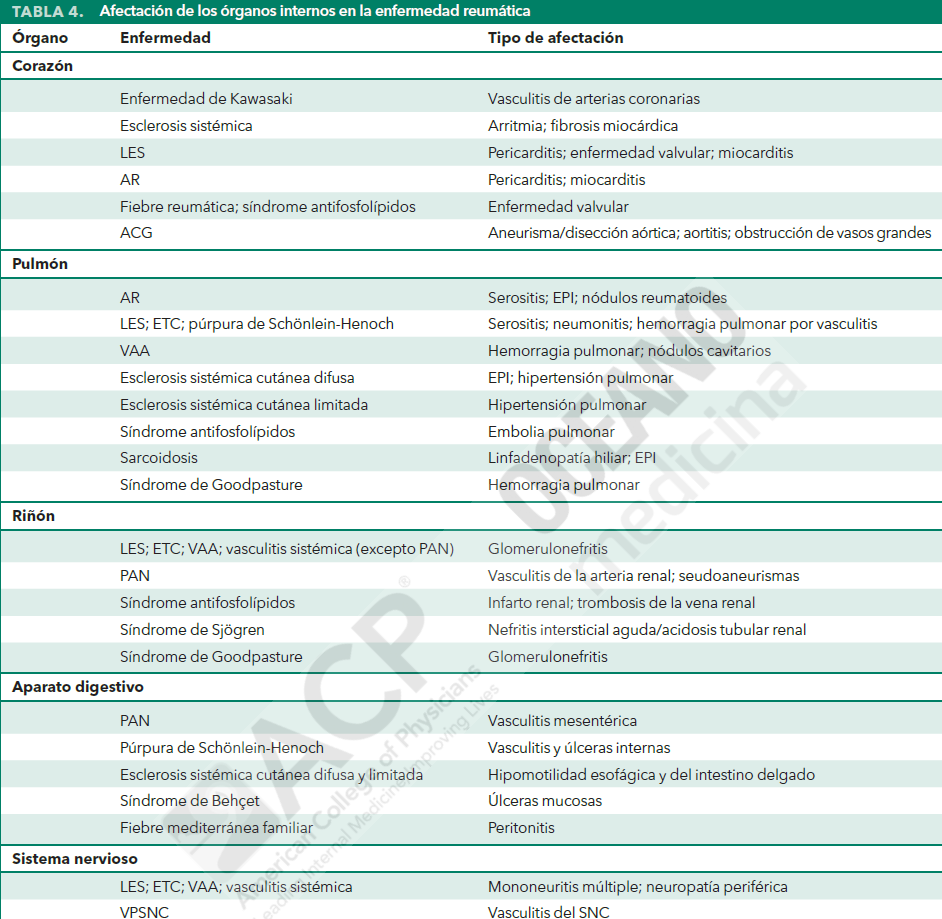
Estudios de laboratorio
Los estudios de laboratorios son útiles para el diagnóstico de las enfermedades reumáticas, ya que permiten identificar la extensión/gravedad de la afectación, evaluar la actividad patológica y controlar las respuestas terapéuticas. Dado que su especificidad es limitada, estas pruebas deben interpretarse siempre en el contexto de la anamnesis clínica y la exploración física y utilizarse con gran precaución, si se utilizan, en el contexto de una baja probabilidad pretest.
Pruebas que miden la inflamación
Velocidad de sedimentación globular
La velocidad de sedimentación globular (VSG) o eritrosedimentación mide la velocidad de caída de los eritrocitos (mm/hora) en un tubo de ensayo con plasma anticoagulado. Los eritrocitos tienden a tener carga negativa en su superficie, lo que da lugar a una repulsión entre ellos y a una VSG prolongada.
El fibrinógeno y otros reactantes de fase aguda neutralizan la carga de la superficie de los eritrocitos y favorece su capacidad de sedimentarse a mayor velocidad. Los niveles altos de fibrinógeno y las VSG elevadas se observa en muchas enfermedades reumáticas tales como las infecciones crónicas y el cáncer.
La VSG normal aumenta con la edad y suele ser más alta en las mujeres. Una regla general aceptada consiste en ajustar el límite superior de la normalidad como edad en años dividida por 2 en los varones y (edad en años + 10)/2 en las mujeres.
Además de los trastornos inflamatorios, pueden observarse VSG elevadas en el embarazo, la diabetes mellitus y la enfermedad renal terminal. Debido a las propiedades reostáticas, la anemia y la macrocitosis también están asociadas a una VSG elevada.
Una VSG excesivamente baja puede darse en estados de fibrinógeno bajo, como la insuficiencia hepática y la cardíaca, y en condiciones que favorecen la formación de pilas de eritrocitos (policitemia vera). La anemia de células falciformes y las microcitosis (incluida la esferocitrocis) también pueden reducir la VSG.
Una VSG notablemente elevada (>100 mm/hora) debe alertar a los médicos sobre trastornos como arteritis de células gigantes, mieloma múltiple, cáncer metastásico u otros estados extremadamente inflamatorios (infecciones o enfermedad autoinmune).
Proteína C reactiva
La proteína C reactiva (PCR) se produce en el hígado principalmente como respuesta a la interleucina (IL)-6 generada por los leucocitos durante el estado inflamatorio. Habitualmente, los niveles de PCR y la VSG siguen un patrón común, pero a menudo la PCR responde con más rapidez a las alteraciones inflamatorias.
En los trastornos reumáticos, la PCR suele estar elevada entre 2 y 10 veces el nivel normal; un nivel más alta (especialmente >10mg/dl [100 mg/l]) debe llevar a considerar un diagnóstico alternativo como la infección.
Se cree que la PCR es un mejor marcador que la VSG para medir inflamación en la espondiloartrosis. En cambio, en algunos pacientes con LES la PCR puede seguir normal a pesar de que la enfermedad esté activa. La PCR puede estar elevada en la obesidad, y una PCR baja puede observarse con el uso de algunos antibióticos y bloqueadores de la IL-6.
Complemento
El sistema de complemento constituye una parte esencial de la respuesta inmunitaria que promueve la vasodilatación, atrae a los leucocitos y favorece la lisis de las bacterias opsonizadas durante la inmunidad humoral.
Los componentes del complemento actúan como reactantes de fase aguda y aumentan en muchos estados inflamatorios. Sin embargo, en respuestas a las enfermedades por formación de inmunocomplejos (LES y vasculitis crioglobulinémica y urticaria) y algunos otros estados, las cascadas del complemento se activan y los niveles de complemento bajan debido al consumo excesivo. Paradójicamente, la deficiencia genética de componentes iniciales del complemento pueden aumentar el riesgo de enfermedades autoinmunes de tipo lúpico.
Los componentes del complemento que se miden de manera habitual son el C3 y el C4. Teniendo en cuenta su coste y su limitada utilidad, el ensayo CH50 no debe realizarse de manera sistemática.
Pruebas de anticuerpos
Las enfermedades reumáticas suelen estar asociadas a autoanticuerpos, pero la presencia de estos no equivale al diagnóstico de una afección subyacente, porque carecen de especificidad y pueden observarse en otros trastornos y en personas sanas.
En los laboratorios comerciales, los análisis de autoanticuerpos se han automatizados con el uso del enzimoinmunoanálisis de adsorción en un algoritmo secuencial, lo que puede simplificar la evaluación del médico pero tiende a ofrecer menores sensibilidad y especificidad.
El Factor reumatoide es un anticuerpo tipo inmunoglobulina M (IgM) dirigido contra la porción Fc de la inmunoglobulina G (IgG). Aunque esta asociado especialmente a AR, el factor reumatoide se encuentra presente en menos del 70% de los pacientes con AR y es frecuente en otras enfermedades.
Los anticuerpos antipéptidos citrulinado cíclico son más específicos de la AR, pero menos sensible. La presencia de ambos autoanticuerpos juntos aumente la probabilidad de AR.
Los anticuerpos antinucleares (ANA) están dirigidos contra los antígenos nucleares y tradicionalmente están asociados a LES. En torno a una tercera parte de la población sana tiene un título bajo (1:40) de ANA, y entre el 3% y 5% presenta un título de 1:160 o más.
Los ANA pueden observarse también en otros trastornos autoinmunes, infección y cáncer, y pueden estar inducidos por fármacos. Un ANA positivo aislado con síntomas inespecíficos y una exploración clínica normal no demuestra el diagnóstico de una enfermedad del tejido conectivo.
Un título alto de ANA está asociado más a menudo a una enfermedad reumática subyacente, aunque no siempre a LES. Sin embargo, casi la totalidad de los pacientes con LES (>95%) tienen ANA positivo. El título de ANA no está correlacionado con la actividad patológica y no debe usarse para evaluar la actividad.
Las pruebas específicas de ANA o pruebas de subserología (es decir, las pruebas de anticuerpos contra componentes nucleares específicos como el ADN o los centrómeros) deben reservarse para los pacientes con ANA positivo y un síndrome clínico indicativo de una enfermedad subyacente del tejido conectivo.
No deben llevarse a cabo pruebas de subserología de ANA de manera rutinaria, ni siquiera en el contexto de ANA positivo, si no hay una fuerte sospecha clínica de una enfermedad subyacente del tejido conectivo.
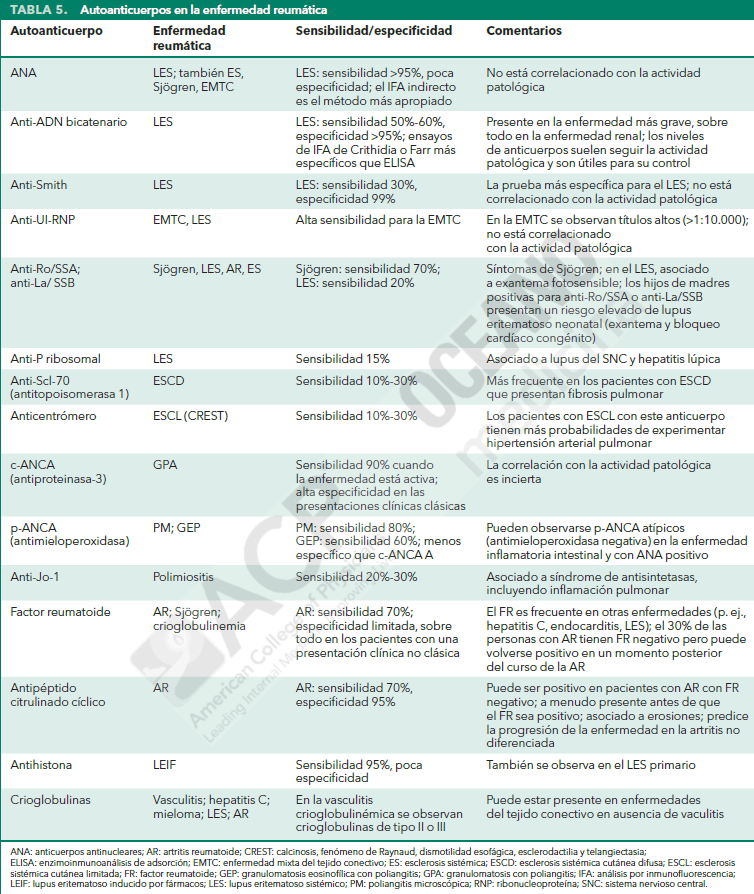
Estudios de imagen
Radiografía
La Rx simple constituye una modalidad esencial para la evaluación de numerosas enfermedades reumáticas y permite evaluar y diferencias la artritis inflamatoria, la artrosis y las artropatías por cristales.

La radiografía simple tiene limitaciones debido a que ofrece una imagen bidimensional de estructuras tridimensionales, es limitada en cuanto a la capacidad de visualizar las partes blandas y pueden no detectar alteraciones erosivas iniciales o de pequeño tamaño.
A pesar de estas limitaciones, la radiografía simple suele ser la primera prueba de imagen que se solicita en la evaluación de las enfermedades reumáticas, porque es económica y fácil de obtener, sólo expone a los pacientes a un nivel bajo de radiación ionizante y es útil para controlar la progresión de la artritis.
Tomografía computarizada
La tomografía computarizada (TC) ofrece varias proyecciones y orientaciones en único estudio, pero es más útil para las anomalías óseas que para la inflamación de partes blandas o las colecciones de líquido.
La TC es más sensible para detectar erosiones óseas que las radiografías simple que la resonancia magnética (RM). Sin embargo, la TC es más cara que la radiografía y expone más a radiación al paciente.
Resonancia magnética
La RM es la técnica radiológica de uso habitual más sensible para detectar anomalías de partes blandas, inflamación y colecciones de líquido, pero es menos eficaz que la TC para demostrar anomalías o erosiones óseas.
La RM es sensible para detectar inflamación inicial en la columna y las articulaciones sacroilíacas y puede estar indicada para la evaluación de una presunta espondiloartritis si las radiografías simples son negativas.
La RM no expone a radiación al paciente, pero tiene un coste elevado, su disponibilidad es limitada y está asociada a una posible intolerancia del paciente debido a la claustrofobia o al hábito corporal.
Ecografía
El uso de la ecografía para evaluar a los pacientes con enfermedades reumáticas se ha incrementado de forma espectacular en los últimos 10 años.
La ecografía es relativamente barata, permite explorar estructuras tridimensionales y ofrece datos en tiempo real en la clínica sin exponer al paciente a radiación ionizante.
Permite evaluar anomalías de partes blandas tales como sinovitis, tendinitis, bursitis y derrames, así como valorar la actividad patológica mediante Doppler, y facilita las inyecciones en tendones o articulaciones. Sin embargo, depende del operador y la competencia exige formación y práctica.
Artrocentesis
La artrocentesis (aspiración articular) y el análisis de líquido sinovial son esenciales para diferenciar entre derrames inflamatorios y no inflamatorios o para distinguir entre artritis infecciosa y artropatías agudas por cristales.
En la evaluación de cualquier monoartritis o cuando se considera una infección, es necesario efectuar una artrocentesis para diagnosticar la causa subyacente. El líquido sinovial aspirado debe enviarse a laboratorio para recuento leucocitario, tinción de GRAM y cultivos, así como para una evaluación de cristales con luz polarizada.
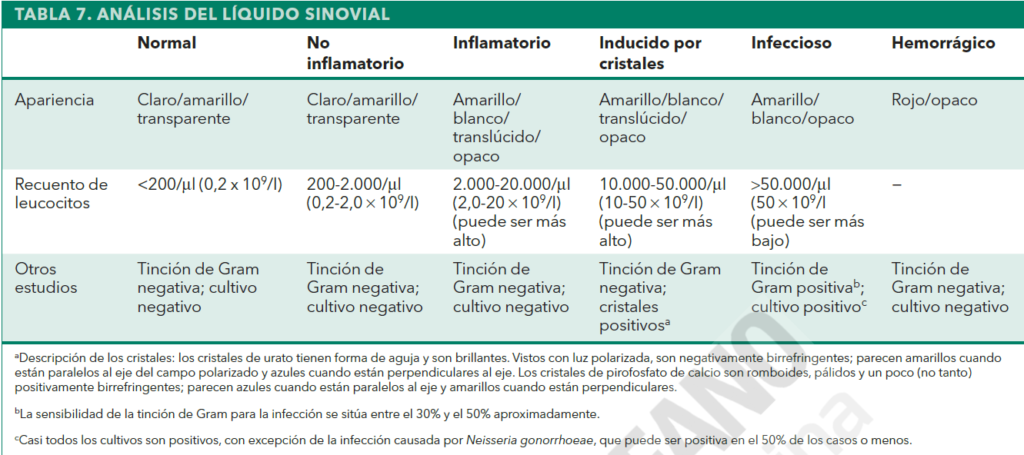
No hay un valor límite absoluto de la cifra de leucocitos en el líquido sinovial para descartar artritis infecciosa; sin embargo, recuentos >50,000/ul con predominio de células polimorfonucleares implican una alta probabilidad de infección.
Normalmente, recuentos <2.000/ul están asociados a etiologías no inflamatorias. Cabe destacar que los cristales pueden coexistir con infección y que su presencia no descarta infección si el grado de sospechas alto.
Biopsia tisular
Si procede, la biopsia de tejidos de órganos afectados puede ser útil para diagnosticar numerosos trastornos reumáticos, como la vasculitis (biopsia de pulmón, riñón o arteria temporal) y el LES (biopsia cutánea).
La biopsia tisular puede ayudar también a evaluar la actividad patológica ((biopsia renal en el LES). Es necesario sopesar adecuadamente los beneficios con los posibles riesgos del procedimiento.
Principios terapéuticos
Agentes antiinflamatorios
Glucocorticoides
Los glucocorticoides son eficaces en numerosas enfermedades reumáticas, entre las que se encuentra la AR, la artropatía aguda por cristales, la vasculitis sistémica, la polimialgia reumática, el LES, las miopatías inflamatorias y las enfermedades auto inflamatorias.
Sus ventajas son un inicio de acción rápido, la facilidad de uso, el bajo costo y su disponibilidad universal; en muchos estados patológicos, son modificadores de la enfermedad y a veces pueden salvar la vida.
Los glucocorticoides tienen numerosos efectos adversos, que son más probables con dosis altas y tratamientos prolongados. Entre tales efectos adversos se incluyen osteoporosis, inmunosupresión, fragilidad cutánea, glaucoma, cataratas, aumento de peso, diabetes mellitus, hipertensión, agitación psicomotora, osteonecrosis e inhibición del eje hipotálamo-hipófisis-suprarrenal.
En los pacientes que tienen previsto tomar más de 2.5 mg de prednisona durante más de tres meses es necesario evaluar el riesgo de osteoporosis inducida por glucocorticoides y procurar un manejo adecuado, quienes presenten un riesgo moderado o alto de fracturas osteoporóticas y reciban un tratamiento con glucocorticoides a largo plazo deben iniciar bifosfonatos orales.
Antiinflamatorios no esteroideos
Los antiinflamatorios no esteroideos (AINE) previenen la producción de prostaglandina mediante la inhibición de las dos isoformas de la ciclooxigenasa (COX), COX-1 y COX-2.
La COX-2 es una enzima inducible que se expresa normalmente en medios inflamatorios, mientras que la COX-1 se expresa de manera constitutiva y ayuda a mantener la homeostasis del organismo.
Casi todos los inhibidores de la COX disponibles son no selectivos (inhiben las dos isoenzimas), reduciendo la producción de prostaglandinas en los estados inflamatorios e interfiriendo en las funciones de mantenimiento de los prostaonides (en el flujo sanguíneo renal y el mantenimiento de la integridad de la mucosa intestinal).

Los inhibidores no selectivos de la COX inhiben también el tromboxano A2, por lo que inhiben la función trombocítica
y favorecen la hemorragia. A pesar de que alivian los síntomas, los inhibidores de la COX no modifican la enfermedad, con la excepción aparente de la espondilitis anquilosante.
Los principales problemas de los inhibidores de la COX son el aumento del riesgo de hemorragia gastrointestinal (sobre todo en las personas que ya están en riesgo) y de eventos adversos cardiovasculares; por lo tanto, deben prescribirse a la dosis más baja y durante el menor tiempo posible.
En general, los inhibidores de la COX deben evitarse en los pacientes con anticoagulación concomitante. Los inhibidores selectivos de la COX-2 se desarrollaron para preservar la COX-1 y reducir el riesgo gastrointestinal; aunque son eficaces para este fin, se observó que la mayoría de los inhibidores selectivos de la COX-2 aumentan el riesgo de eventos cardiovasculares y fueron retirados del mercado.
Los AINE varían en cuanto a cinética, selectividad para la COX-1/2 y otras características, y conllevan grados de riesgo
algo diferentes; la experiencia con varios AINE distintos puede ser beneficiosa en la práctica clínica. Los AINE tópicos como el diclofenaco están disponibles bajo prescripción médica para la artritis y suponen un menor riesgo de efectos secundarios sistémicos que los AINE orales.
Pueden ser preferibles en los pacientes con un riesgo elevado de efectos adversos de los AINE orales y/o en las personas
≥75 años de edad. Sin embargo, suelen ser caros.
Colchicina
La colchicina inhibe los microtúbulos y altera la función de los neutrófilos. En la mayoría de los casos, se utiliza para la gota y la artritis aguda por cristales de pirofosfato de calcio (seudogota). También se usa para tratar la vasculitis por hipersensibilidad y la fiebre mediterránea familiar.
Son frecuentes los efectos secundarios gastrointestinales (especialmente la diarrea). En caso de sobredosis, puede producirse una mielodepresión grave (incluso mortal). En caso de enfermedad renal, es necesario ajustar la dosis.
Cuando se administra de manera prolongada, la colchicina puede provocar en contadas ocasiones toxicidad neuromuscular, sobre todo si se administra conjuntamente con fármacos estatínicos.
Debe evitarse la administración concomitante de inhibidores fuertes del CYP3A4 (claritromicina), que reducen el catabolismo hepático de la colchicina.
Analgésicos y moduladores de la vía del dolor
Paracetamol
La eficacia del paracetamol para la artrosis y el dolor lumbar está cada vez más cuestionada, con ensayos controlados y
metaanálisis recientes que demuestran la ausencia de beneficio del fármaco, incluso a dosis altas (3.000-4.000 mg/día).
Tramadol
El tramadol es un analgésico opiáceo mixto y un inhibidor débil de la recaptación de serotonina y noradrenalina. Su potencial de adicción es menor que el de los opiáceos tradicionales, que en general se evitan en el tratamiento reumatológico.
Duloxetina
La duloxetina es un inhibidor de la recaptación de serotonina y noradrenalina aprobado por la Food and Drug Administration (FDA) de Estados Unidos para el manejo del dolor musculoesquelético crónico y la fibromialgia.
Ofrece un alivio moderado del dolor para la artrosis de rodilla, el dolor lumbar crónico y la fibromialgia. Cuando se suspende su utilización, es necesario reducir la dosis gradualmente para evitar los síntomas de abstinencia.
Gabapentinoides
Los gabapentinoides (gabapentina y pregabalina) inhiben los canales de calcio activados por voltaje, por lo que reducen la transmisión de la señal del dolor. La pregabalina está aprobada por la FDA para la fibromialgia.
Los frecuentes efectos secundarios (mareo, desequilibrio, somnolencia, aumento de peso, edema periférico, dificultades cognitivas) pueden limitar su utilidad, y a veces está justificada su suspensión.
La gabapentina también mejora moderadamente los síntomas de fibromialgia, con un perfil de efectos secundarios parecido.
Fármacos antirreumáticos modificadores de la enfermedad
Fármacos antirreumáticos modificadores de la enfermedad no biológicos
En la siguiente Tabla se resumen los mecanismos de acción, las indicaciones y los parámetros de control habituales de diversos fármacos antirreumáticos modificadores de la enfermedad (FARME) no biológicos.
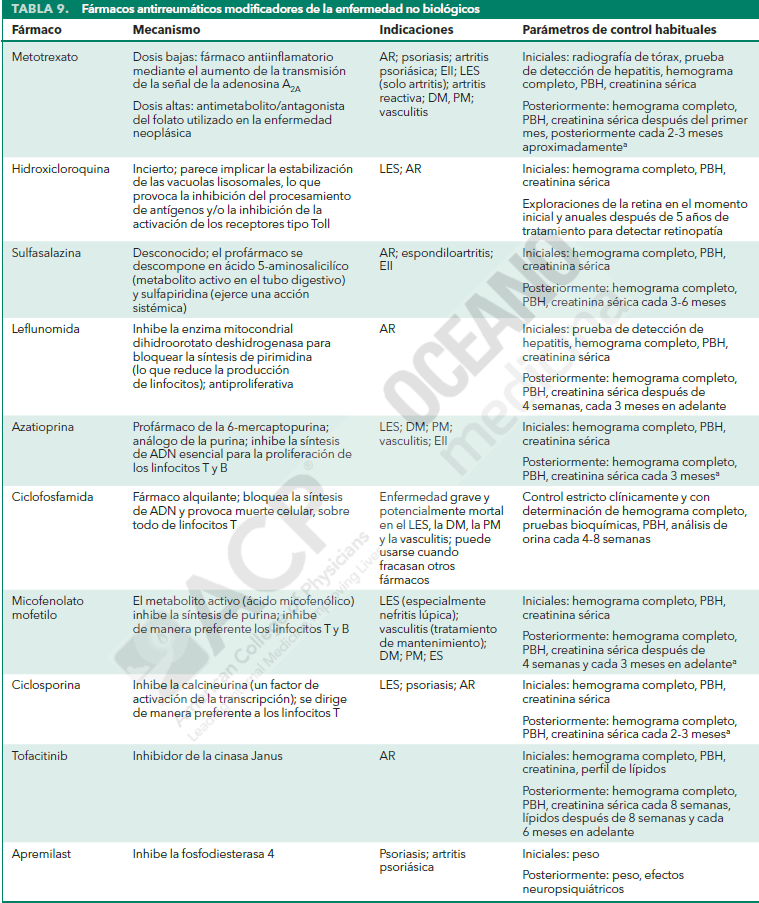
Metotrexato
El metotrexato es un medicamento de primera línea para el tratamiento de la AR y otras enfermedades autoinmunes. Normalmente, se administra una dosis semanal de entre 10 y 25 mg por vía oral o subcutánea.
A dosis superiores a 15 mg, la administración parenteral es más fiable, si bien es mucho más cara. Los posibles efectos secundarios son cefaleas, fatiga y náuseas (sobre todo en torno al momento de la administración semanal).
Puede provocar hepatotoxicidad y citopenias (especialmente anemia macrocítica), y en caso de enfermedad renal es necesario ajustar la dosis.
El metotrexato debe evitarse en los pacientes con enfermedad hepática o renal significativa. Los suplementos de ácido fólico minimizan la toxicidad a la vez que preservan la eficacia. Se recomienda limitar el consumo de alcohol.
Hidroxicloroquina
La hidroxicloroquina es un inmunomodulador que se usa de manera generalizada en el LES, en el que reduce la mortalidad y la probabilidad de experimentar nefritis. Rara vez es suficiente como monoterapia para la AR, pero es útil como tratamiento complementario.
Sulfasalazina
La sulfasalazina se utiliza para el tratamiento de la AR y la artritis psoriásica no axial, aunque su uso ha disminuido debido
a la relativa eficacia del metotrexato y la leflunomida. En la actualidad se emplea sobre todo como parte de un tratamiento combinado de FARME para la AR y en las mujeres que se plantean quedarse embarazadas. Los efectos secundarios graves son discrasias sanguíneas, hepatitis y reacciones de hipersensibilidad.
Dado su efecto beneficioso en la enfermedad inflamatoria intestinal (EII), puede constituir una estrategia
útil para los pacientes con artritis asociada a EII.
Leflunomida
La leflunomida está aprobada por la FDA para la artritis reumatoide y psoriásica, con una eficacia parecida a la del metotrexato. Es necesario controlar en los pacientes que reciben este fármaco la aparición de hepatotoxicidad y mielodepresión.
Otros efectos secundarios frecuentes son náuseas, cefaleas, exantema, diarrea y transaminitis. La neuropatía periférica representa un efecto secundario infrecuente, pero normalmente remite de manera espontánea con la suspensión del fármaco.
El metabolito activo de la leflunomida (teriflunomida) tiene una semivida de casi tres semanas; por lo tanto, cuando es necesario eliminar el fármaco con rapidez, hay que realizar un reposo farmacológico o lavado con colestiramina de 11 días.
Azatioprina
La azatioprina es un inmunodepresor que se utiliza en varias enfermedades inflamatorias. Su uso concomitante con inhibidores de la xantina oxidasa (alopurinol, febuxostat) está contraindicado.
El principal efecto adverso de la azatioprina es la mielodepresión. Las pruebas de la enzima tiopurina metiltransferasa
permiten identificar a los pacientes con actividad enzimática reducida o ausente y un riesgo elevado de mielodepresión.
Ciclofosfamida
La ciclofosfamida es un potente inmunodepresor con un inicio de acción rápido (de días a semanas). Se emplea para trata vasculitis, las complicaciones potencialmente mortales del LES y la enfermedad pulmonar intersticial.
En gran parte, la ciclofosfamida ha sido reemplazada por los fármacos más nuevos y seguros en el tratamiento de primera línea de la vasculitis asociada a ANCA y la nefritis lúpica (rituximab y micofenolato mofetilo, respectivamente), pero sigue utilizándose en casos graves o cuando estos fármacos fracasan.
Los posibles efectos secundarios graves son inmunodepresión, leucocitopenia, cistitis hemorrágica e insuficiencia ovárica, así como un riesgo a largo plazo de cáncer de vejiga, leucemia y linfoma.
Micofenolato mofetilo
En la actualidad, el micofenolato mofetilo es el fármaco de primera línea para la nefritis lúpica y puede ser eficaz para la esclerosis sistémica y la enfermedad pulmonar intersticial asociada. Son frecuentes los efectos secundarios gastrointestinales, sobre todo la diarrea. Puede provocar mielodepresión.
Inhibidores de la calcineurina
Entre los inhibidores de la calcineurina se incluyen la ciclosporina y el tacrolimus. Aunque en la actualidad el uso de ciclosporina en reumatología es infrecuente, uno de sus efectos secundarios más habituales es la hiperuricemia, y la gota inducida por ciclosporina es una consideración importante en los pacientes que toman el fármaco y presentan monoartritis aguda.
En estos momentos, el tacrolimus es objeto de un interés renovado como posible tratamiento alternativo para la
nefritis lúpica.
Tofacitinib
El tofacitinib es un fármaco oral que inhibe la vía de señalización de la cinasa Janus (JAK). El tofacitinib está aprobado por
la FDA para la AR y tiene una eficacia equivalente a la de los FARME biológicos. Los riesgos son hiperlipemia, hepatotoxicidad y leucocitopenia.
Apremilast
El apremilast es moderadamente eficaz para la psoriasis y la artritis psoriásica. No provoca inmunodepresión ni mielodepresión. Sin embargo, el apremilast es menos eficaz que los FARME biológicos y tiene un inicio de acción lento; se desconoce su efecto en la progresión del daño erosivo.
Los eventos adversos incluyen efectos secundarios gastrointestinales (principalmente náuseas y diarrea) y pérdida de peso. Debe utilizarse con precaución en los pacientes con antecedentes de depresión.
Fármacos antirreumáticos modificadores de la enfermedad biológicos
Los FARME biológicos son fármacos altamente específicos que se administran por vía parenteral y están basados en proteínas con dianas extracelulares (citocinas proinflamatorias específicas, receptores de citocinas o cúmulos de diferenciación de moléculas de superficie celular en las células inmunitarias).
El final del nombre genérico de un fármaco biológico indica de qué tipo de molécula corresponde: -mab significa anticuerpo monoclonal; -kin indica que es una sustancia de tipo interleucina; -ra corresponde a un antagonista de receptores, y -cept está reservado para las moléculas receptoras.
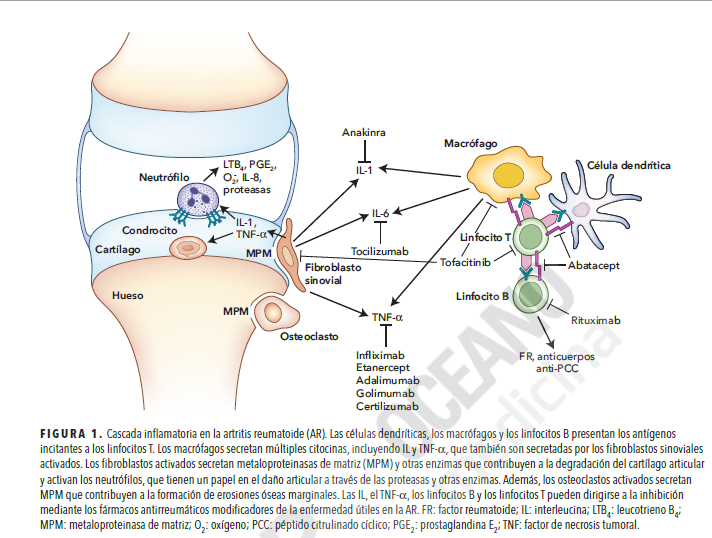
Los FARME biológicos aumentan el riesgo de infección en grados variables. Por lo tanto, es necesario realizar un cribado selectivo antes de iniciarlos. El coste de los fármacos biológicos es significativo y puede suponer un obstáculo para acceder a ellos.
Inhibidores del factor de necrosis tumoral alfa
Los inhibidores del factor de necrosis tumoral alfa (TNF-α) son grandes moléculas basadas en proteínas que deben
administrarse por vía parenteral. Se emplean de manera generalizada para el tratamiento de la AR, la psoriasis, la artritis psoriásica y la espondilitis anquilosante, y están aprobados también para varias enfermedades no reumáticas.
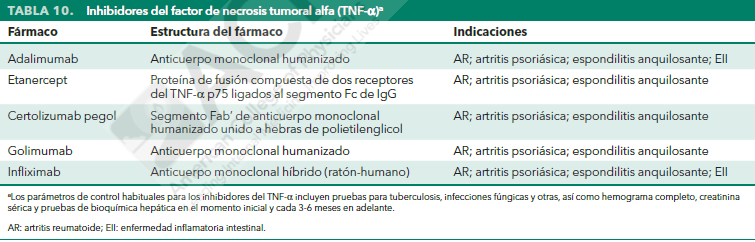
En general, los inhibidores del TNF-α se toleran bien, con un mayor riesgo de infección como principal problema de seguridad. Conllevan un riesgo especialmente alto de reactivación de la tuberculosis, por lo que todos los pacientes en los que se plantee un tratamiento inhibidor del TNF-α deben someterse a un cribado y recibir una profilaxis adecuada.
Los inhibidores del TNF-α no parecen aumentar el riesgo de cánceres nuevos, aparte del cáncer de piel no melanómico y, posiblemente, el melanoma; el riesgo de recidiva neoplásica es incierto.
Estos fármacos pueden agravar también la insuficiencia cardíaca y de manera infrecuente provocan un trastorno desmielinizante. Es frecuente que los inhibidores del TNF-α pierdan eficacia con el tiempo, debido a la formación
de anticuerpos antifármaco.
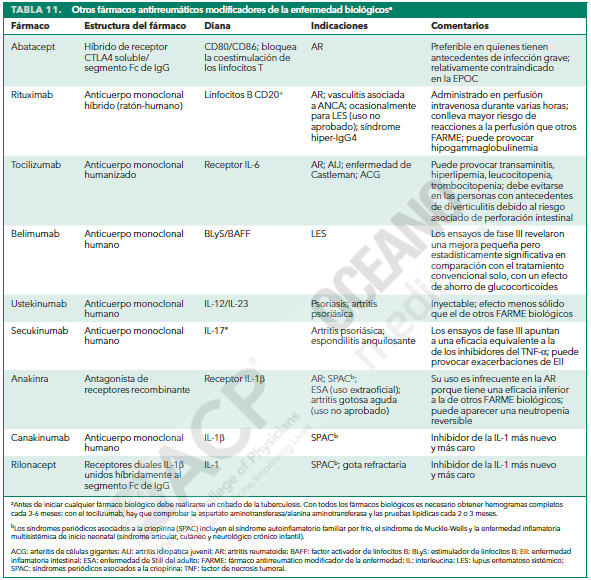
Otros fármacos antirreumáticos modificadores de la enfermedad biológicos
En la última década, la FDA ha aprobado varios FARME con otras dianas extracelulares y de la superficie celular. La mayoría de estos fármacos se inician después del fracaso de uno o dos inhibidores del TNF-α.
Biosimilares
Los fármacos biosimilares son versiones «de imitación» de medicamentos biológicos de marca. No son réplicas exactas (de ahí el término «biosimilares» y no «genéricos»); por lo tanto, deben superar estudios de fase III para obtener la aprobación de las autoridades. En 2016, la FDA aprobó tres biosimilares anti-TNF.
Tratamiento reductor de uratos
Alopurinol
El alopurinol es el fármaco reductor de uratos de uso más frecuente. Inhibe de manera competitiva la enzima xantina oxidasa, por lo que bloquea la conversión de la hipoxantina (un producto de descomposición de las purinas) a ácido úrico.
El alopurinol se metaboliza a oxipurinol, que también inhibe la xantina oxidasa. El alopurinol está aprobado por la FDA a
dosis de hasta 800 mg/día. Según el American College of Rheumatology, el alopurinol debe iniciarse a 100 mg/día para ajustar progresivamente la dosis en incrementos de 100 mg cuando sea necesario; en quienes tengan enfermedad renal crónica en estadio 4 o 5, el alopurinol debe iniciarse a 50 mg/día y ajustarse progresivamente en incrementos de 50 mg cuando sea necesario.
El mayor riesgo del fármaco es el síndrome de reacción farmacológica con eosinofilia y síntomas sistémicos (drug reaction with eosinophilia and systemic symptoms [DRESS]), una reacción infrecuente que suele darse en presencia de enfermedad renal crónica y uso de diuréticos y tiene una tasa de mortalidad elevada.
Recientemente se ha descubierto que el alelo HLA-B5801, que es más frecuente en las personas de ascendencia china han, tailandesa y coreana, es un factor de riesgo de DRESS. Se recomienda el cribado del HLA-B5801 en las poblaciones de alto riesgo antes de iniciar el tratamiento. Los inhibidores de la xantina oxidasa no pueden administrarse conjuntamente con análogos de las purinas (como la azatioprina).
Febuxostat
El febuxostat es un inhibidor no competitivo de la xantina oxidasa. Como con el alopurinol, en raras ocasiones se produce una transaminitis y es necesario controlar las enzimas hepáticas. Está contraindicado el uso con análogos de las purinas. La incidencia del síndrome DRESS es infrecuente.
Fármacos uricosúricos
El probenecid es un inhibidor del transporte de ácidos orgánicos que reduce la recaptación renal de ácido úrico. El probenecid es de uso infrecuente debido a su eficacia limitada, así como a la incomodidad y las limitaciones que comporta su uso.
El lesinurad es un inhibidor de gran potencia de la recaptación renal de ácido úrico dirigido al transportador de urato
URAT1 que se ha aprobado recientemente. Está aprobado solo para uso en combinación con febuxostat o alopurinol. El lesinurad puede provocar toxicidad renal en raras ocasiones y no se debe administrar a quienes presentan un aclaramiento de creatinina <45 ml/min.
Pegloticasa
A diferencia de la mayoría de los demás mamíferos, los seres humanos carecen de una uricasa activa que descomponga el ácido úrico. La pegloticasa es una uricasa pegilada recombinante no humana perfundible con una gran eficacia para reducir el urato sérico.
La pegloticasa se reserva para la gota grave y/o refractaria. Dada su potencia extrema, son frecuentes las exacerbaciones de la gota por movilización, y es necesaria una profilaxis contra las crisis agudas de gota. La pegloticasa se administra por vía intravenosa cada dos semanas; si el nivel de urato sérico anterior a la perfusión aumenta a más de 6,0 mg/dl (0,35 mmol/l) en dos ocasiones, es probable que se hayan formado anticuerpos y hay que suspender el fármaco para evitar reacciones a la perfusión.
Medicamentos y embarazo
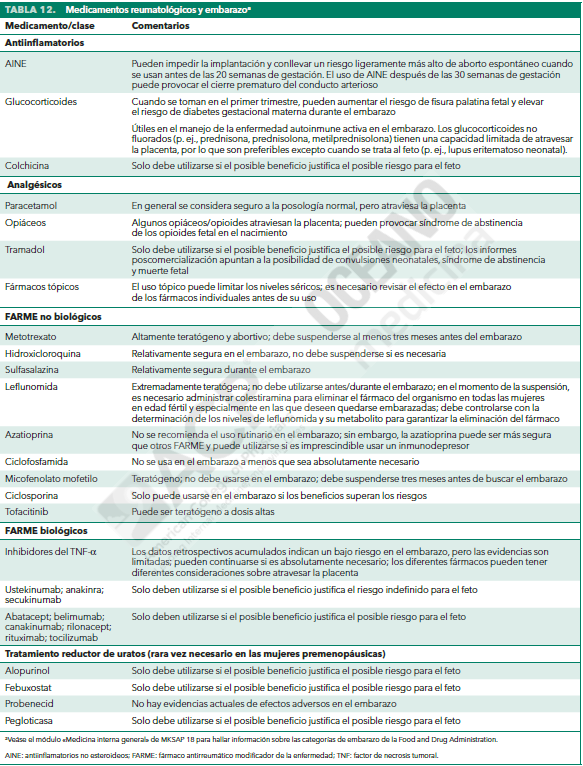
Algunos medicamentos usados en trastornos reumáticos pueden tener efectos adversos en el embarazo.
Vacunación y cribado en la inmunodepresión
Los pacientes deben estar al día de las vacunas antes de iniciar los regímenes de FARME biológicos. La respuesta vacunal
puede disminuir una vez iniciado el tratamiento, y los pacientes en tratamiento con algunos inmunodepresores (incluidos
todos los FARME biológicos y el tofacitinib) no deben recibir vacunas con virus vivos atenuados (como las del herpes
zóster, la gripe con virus vivos atenuados y la fiebre amarilla) debido al riesgo de actividad vírica en el huésped inmunodeprimido.
A pesar de la menor eficacia, los pacientes con un FARME biológico deben recibir cualquier vacuna sin virus vivos que esté indicada según los protocolos habituales. Los pacientes que reciban FARME orales tradicionales (hidroxicloroquina,
metotrexato y sulfasalazina) pueden recibir cualquiera y todas las vacunas necesarias.
Antes de iniciar un tratamiento inmunodepresor, se recomiendan los cribados siguientes:
- Cribado de la tuberculosis con la prueba de la tuberculina
o el ensayo de liberación de interferón gamma, especialmente
en los pacientes que inicien FARME biológicos. - Pruebas serológicas de las hepatitis B y C (para los FARME
biológicos y los fármacos que puedan provocar hepatotoxicidad). - Cribado del VIH.
Los pacientes con tuberculosis latente o activa, hepatitis B activa o infección por VIH no tratada deben iniciar el tratamiento adecuado antes de empezar con la inmunodepresión.
En caso de factores de riesgo de exposición continuada a la tuberculosis, el cribado de la tuberculosis debe realizarse
anualmente.
Manejo no farmacológico y no tradicional
Dado que las enfermedades reumáticas afectan con frecuencia al sistema musculoesquelético, muchas veces se utilizan
medidas no farmacológicas para abordar el dolor que no eliminan los medicamentos. Entre tales medidas se incluyen fisioterapia, terapia ocupacional, cirugía, pérdida de peso, apoyo psicosocial y programas de automanejo.
Muchos pacientes recurren a la medicina complementaria y alternativa como complemento a las intervenciones médicas tradicionales.
Fisioterapia y terapia ocupacional
El fisioterapeuta puede ayudar al profesional de atención primaria a evaluar el estado físico aeróbico y el acondicionamiento de un paciente, así como la capacidad de realizar actividades de la vida diaria. El dolor y la limitación funcional pueden abordarse con terapias manuales, dispositivos de asistencia, técnicas de protección articular y tratamientos térmicos.
Puede iniciarse un programa de ejercicios dirigidos; su adaptación es fundamental para el uso domiciliario. La tendinitis, la bursitis, muchas formas de artritis y el dolor crónico de partes blandas debido a sobrecarga, lesión y síndromes de dolor crónico (como la fibromialgia) se encuentran entre los diagnósticos apropiados para la derivación a fisioterapia.
Los terapeutas ocupacionales evalúan el funcionamiento de las extremidades superiores, incluida la capacidad de llevar a cabo las tareas de cuidados personales y laborales. Pueden ofrecerse fajas y férulas para las articulaciones dolorosas o inestables.
Una evaluación ergonómica del lugar de trabajo puede acompañar la formación para mejorar la mecánica corporal y evitar los traumatismos repetidos.
Medicina complementaria y alternativa
Aproximadamente la tercera parte del total de los pacientes y hasta el 90% de los pacientes con dolor crónico, como el derivado de artritis o enfermedades reumáticas, utilizan opciones no tradicionales para el manejo de los síntomas. Los suplementos sin prescripción médica de uso más frecuente son el aceite de pescado, las vitaminas, la glucosamina y la
condroitina.
Los profesionales deben preguntar por el uso de suplementos, porque los pacientes rara vez dan esta información de manera espontánea. Pueden producirse interacciones farmacológicas significativas; por ejemplo, algunos preparados fitoterapéuticos pueden interactuar con los anticoagulantes.
Las intervenciones de mente y cuerpo como el taichí, la meditación y el yoga pueden mejorar el bienestar psicológico,
la fuerza, el equilibrio y el nivel de dolor. La manipulación quiropráctica y osteopática, así como el masaje, siguen siendo
populares.
Los ensayos controlados aleatorizados respaldan el uso de taichí para la artritis; ensayos más pequeños indican que las técnicas de meditación, el yoga, el masaje y la medicina manipulativa pueden ser beneficiosos para diversos problemas musculoesqueléticos.
Función de la cirugía
Intervenciones quirúrgicas como la liberación del túnel carpiano o la reparación del tendón del manguito de los rotadores pueden abordar afecciones que tienen su origen en traumatismos repetidos, lesión y alteraciones degenerativas de partes blandas.
En ocasiones se emplea la sinovectomía para eliminar el pannus inflamatorio cuando una articulación o un número limitado de articulaciones de un paciente con AR no responden a los medicamentos. La artroplastia total, sobre todo de rodilla o cadera, puede reducir o eliminar el dolor y restaurar el funcionamiento en los pacientes con una respuesta insuficiente a la medicación y la fisioterapia o la terapia ocupacional.